O que é e o que estuda a Química Geral
A Química Geral é responsável por estudar desde os elementos químicos até as substâncias formadas por eles. Ela engloba assuntos como: o estudo do átomo, as ligações químicas, o estado físico da matéria e a separação de misturas, sendo a base para o estudo de todas as vertentes da Química, como por exemplo a Orgânica.
O átomo
O átomo é a unidade básica da matéria. Para compreender todos os fenômenos químicos, necessita-se conhecer como o átomo está disposto. Logo, o estudo do átomo envolve todas as teorias e publicações que ocorreram ao longo do tempo para se entender a constituição adotada atualmente em que um átomo é composto por: prótons e nêutrons presentes em um núcleo com carga positiva, envoltos por elétrons de carga negativa atraídos ao núcleo por uma força eletromagnética.
Elemento químico

O elemento químico é o conjunto de átomos que apresenta o mesmo número de prótons, ou seja, possuem o mesmo número atômico. Atualmente, existem aproximadamente 118 elementos químicos em que alguns são obtidos naturalmente e outros de modo artificial. Além disso, os elementos possuem propriedades periódicas (dependem do número atômico) e aperiódicas (não dependem do número atômico).
Tabela Periódica
A organização dos elementos químicos existentes se dá por meio da tabela periódica em que os elementos estão dispostos em ordem crescente de número atômico, sendo que cada elemento é representado por uma sigla única. Essa organização distribui os elementos em períodos e famílias.
Ligações Químicas
As ligações químicas ocorrem entre átomos para que uma molécula seja originada. Elas podem ser divididas em: iônica, covalente e metálica, sendo estudadas na Química Geral por serem a base para a compreensão em Química.
O estudo das ligações químicas permite conhecer e prever os comportamentos e propriedades de uma dada substância.
Estados Físicos da matéria
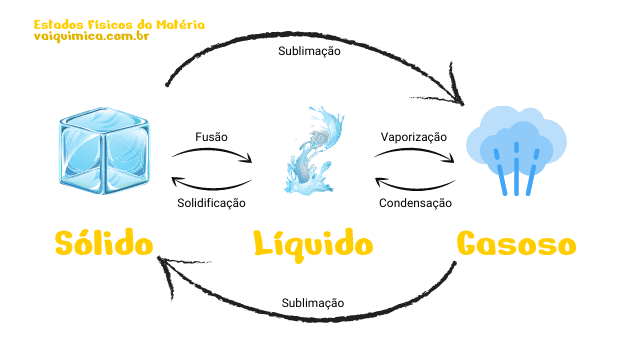
O estudo dos estados físicos da matéria proporciona o entendimento da organização, em escala macroscópica, das moléculas que constituem a matéria. Cada estado físico relaciona-se à proximidade das partículas constituintes das substâncias e podem ser divididos, de maneira geral, em: sólido, líquido e gasoso.
Separação de misturas
A separação das misturas é utilizada para promover a separação de duas ou mais substâncias diferentes que estejam presentes em uma mistura. As misturas podem ser homogêneas ou heterogêneas e o modo de separação depende das características de cada solução.
O que mais cai em Química Geral no ENEM?
A Química Geral também está presente em diferentes provas de vestibulares, inclusive no ENEM. Assim, é importante dominar os assuntos que mais caem para arrasar na prova e garantir sua vaga na universidade.
Mas afinal, quais os temas que mais caem?
Substâncias simples e misturas
Nessa temática, é importante conhecer as características das substâncias puras e das misturas e suas propriedades. Entender os tipos de misturas (heterogênea e homogênea), saber calcular a concentração e principalmente, conhecer e identificar diferentes métodos de separação de misturas.
Dentre os métodos que mais costumam aparecer temos: a decantação, a filtração e a destilação simples e fracionada.
Ligações químicas
Em geral, as ligações químicas costumam aparecer contextualizadas com o comportamento das moléculas de uma determinada substância. Desse modo, é preciso compreender as características das ligações iônicas, covalentes e metálicas e relacioná-las com propriedades como solubilidade, ponto de fusão e de ebulição e também a dissociação e ionização.
Geometria molecular, polaridade e forças intermoleculares
Assim como acontece com as ligações químicas, a temática de geometria molecular, polaridade e forças intermoleculares costumam aparecer contextualizadas para o entendimento de determinadas propriedades, principalmente, solubilidade e ponto de fusão e ebulição.
Logo, torna-se importante conhecer os tipos de geometria molecular, as características das moléculas polares e apolares, assim como as ligações polares e apolares e os diferentes tipos de forças intermoleculares.
Leis ponderais e estequiometria
Por fim, podemos citar as questões de estequiometria. Essas questões são mais matemáticas e solicitam o cálculo da quantidade de reagentes e produtos das reações químicas relacionando-se com as Leis Ponderais como a Lei de Proust, de Dalton e de Lavoisier.








