Prova amarela
Usando um densímetro cuja menor divisão da escala, isto é, a diferença entre duas marcações consecutivas, é de 5,0 x 10-2 g cm-3 , um estudante realizou um teste de densidade: colocou este instrumento na água pura e observou que ele atingiu o repouso na posição mostrada.
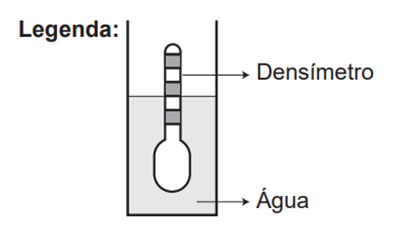
Em dois outros recipientes A e B contendo 2 litros de água pura, em cada um, ele adicionou 100 g e 200 g de NaCl, respectivamente.
Quando o cloreto de sódio é adicionado à água pura ocorre sua dissociação formando os íons Na+ e Cl–. Considere que esses íons ocupam os espaços intermoleculares na solução.
Nestes recipientes, a posição de equilíbrio do densímetro está representada em:
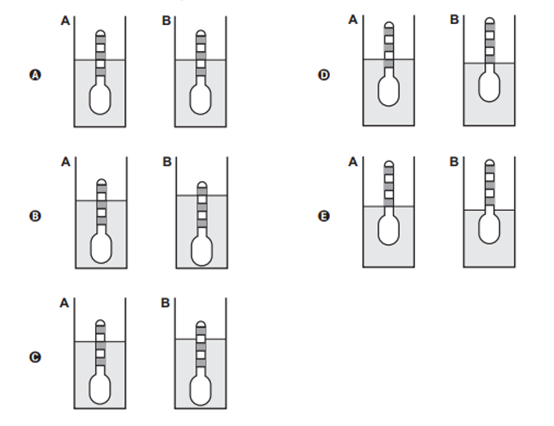
Resolução
Como os íons ocupam espaços intermoleculares, o volume total da mistura é igual ao volume inicial da água.
As densidades das misturas em A e B são dadas de acordo com a equação a seguir:
μA.= massa total/2000
Sendo assim:
μA.= mágua/2000 + 100/2000
μ B.= mágua/2000 + 200/2000
Com essas equações, tem-se:
μA.= mágua /2000 + 5 x 10-2 (g/ cm3)
μB.= mágua /2000 + 10 x 10-2 (g/ cm3)
Diante disso, para o recipiente A, a densidade do líquido aumentou em 5 x 10-2 g/ cm3e sendo assim, deverá subir uma unidade na escala do densímetro. Já para o recipiente B, o líquido aumentou em 10 x 10-2 g/ cm3 e assim, o densímetro deve subir duas unidades.
Resposta: D







