Prova amarela
A minimização do tempo e custo de uma reação química, bem como o aumento na sua taxa de conversão, caracterizam a eficiência de um processo químico. Como consequência, produtos podem chegar ao consumidor mais baratos. Um dos parâmetros que mede a eficiência de uma reação química é o seu rendimento molar (R, em %) definido como
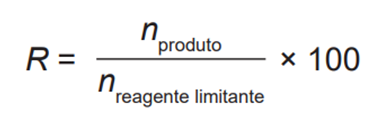
em que n corresponde ao número de mols. O metanol pode ser obtido pela reação entre brometo de metila e hidróxido de sódio, conforme a equação química:
CH3Br + NaOH → CH3OH + NaBr
As massas molares (em g/mol) desses elementos são: H = 1; C = 12; O = 16; Na = 23; Br = 80.
O rendimento molar da reação, em que 32 g de metanol foram obtidos a partir de 142,5 g de brometo de metila e 80 g de hidróxido de sódio, é mais próximo de
(a) 22%.
(b) 40%.
(c) 50%.
(d) 67%.
(e) 75%.
Resolução
Inicialmente, se faz necessário calcular as massas molares dos reagentes:
CH3Br → 95 g/mol
NaOH → 40 g/ mol
Em seguida, calcula-se o número de moles de cada um deles:
CH3Br → 142,5 / 95 = 1,5 mol
NaOH → 80/ 40 = 2 mol
Considerando a reação apresentada:
CH3Br + NaOH → CH3OH + NaBr
1 mol 1 mol
1,5 mol 1,5 mol
Diante disso, nota-se que o NaOH está em excesso já que se adicionou 2 moles e usou-se apenas 1,5 moles, sendo o reagente limitante o CH3Br.
Quanto ao produto formado, tem-se:
Massa molar CH3OH → 32 g/ mol
Número de mol formado → 32/ 32 = 1 mol
Desse modo, calcula-se o rendimento:
R = nproduto/ nreagente limitante x 100 = (1/ 1,5) x 100 = 66,7% = ~67%
Resposta: D








