O que são misturas?
Substância pura
Para entender melhor o que são misturas homogêneas e heterogêneas é necessário definir primeiro o que são substâncias puras.
A definição de substância pura, como o próprio nome diz, indica que a substância não está misturada com uma outra substância. Por exemplo, quando falamos da água, estamos nos referindo a uma substância pura, uma vez que ela não está misturada a mais nada. De modo geral, correspondem a átomos ou moléculas iguais em uma determinada porção da matéria e que apresentam propriedades físicas e químicas próprias. Essas substâncias podem ser classificadas em simples e compostas.
Substância simples
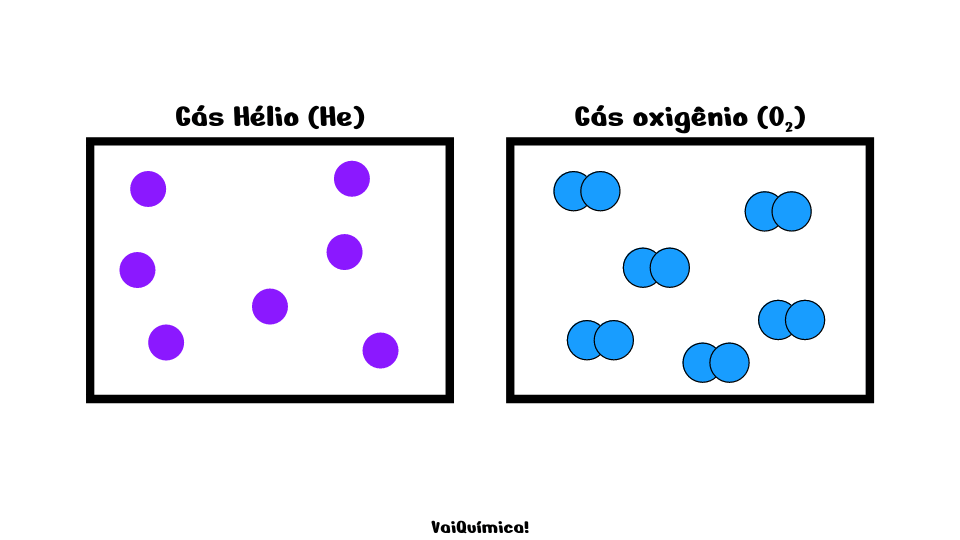
As substâncias puras simples são compostas por um ou mais átomos de um mesmo elemento. Como um exemplo para elucidação, um recipiente contendo O2 apresenta apenas um tipo de molécula formada por apenas um tipo de átomo, no caso, o oxigênio. O mesmo vale para um recipiente contendo apenas gás hélio, há apenas um tipo de átomo envolvido.
Substância composta
Diferentemente das substâncias simples, as substâncias puras compostas abrangem as moléculas formadas por mais de um tipo de elemento químico. No caso a água mencionada inicialmente é classificada como uma substância pura composta pois é formada por átomos de hidrogênio e oxigênio. O mesmo vale para o gás carbônico (CO2) que apresenta essa classificação por ser formado por átomos de carbono e de oxigênio.

Misturas
A mistura corresponde à ‘junção’, ou melhor, a adição de duas ou mais substâncias puras. No momento em que elas são adicionadas ao mesmo recipiente, as substâncias puras deixam de ser consideradas puras e passam a ser componentes de uma mistura.
No entanto, as misturas não são sempre iguais. Quando falamos de misturas, precisamos entender a peculiaridade de cada tipo. Por isso, elas podem ser divididas em: heterogênea e homogênea.
As misturas “clássicas” estudadas para exemplificar cada um dos tipos são: mistura de água com óleo e mistura de água com sal.
Percebe-se que na mistura de água e óleo, o aspecto não é uniforme onde verifica-se a existência de mais de uma fase. Já a mistura de água e sal, apresenta um aspecto uniforme em toda a sua extensão (uma única fase).
Misturas homogêneas
Quando falamos de mistura homogênea, falamos das misturas que apresentam as mesmas propriedades em todos os seus pontos, ou seja, em toda a sua extensão e que possuam apenas uma fase como acontece com a mistura de água e sal. As misturas homogêneas também são conhecidas como soluções.
Misturas heterogêneas
A mistura heterogênea apresenta duas ou mais fases em que cada uma das fases irá apresentar características bem definidas e distintas entre si, como ocorre com a mistura de água e óleo.
No entanto, nem todas as misturas heterogêneas podem ser classificadas assim a olho nu. Há alguns casos em que a identificação de mais de uma fase no sistema só pode ser verificada com a utilização de microscópios. O que acontece é que nesse tipo de mistura visualiza-se partículas em suspensão e são denominadas colóides. Alguns exemplos são: o sangue, o leite, a maionese, tintas, entre outros.








