Prova azul
O ácido acetilsalicílico, AAS (massa molar igual a 180 g/mol), é sintetizado a partir da reação de ácido salicílico (massa molar igual a 138 g/mol) com anidrido acético, usando-se ácido sulfúrico como catalisador, conforme a equação química:
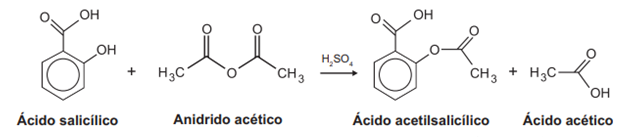
Após a síntese, o AAS é purificado e o rendimento final é de aproximadamente 50%. Devido às suas propriedades farmacológicas (antitérmico, analgésico, anti-inflamatório e antitrombótico), o ASS é utilizado como medicamento na forma de comprimidos, nos quais se emprega tipicamente uma massa de 500 mg dessa substância.
Uma indústria farmacêutica prefere fabricar um lote de 900 mil comprimidos, de acordo com as especificações do texto. Qual é a massa de ácido salicílico, em kg, que deve ser empregada para esse fim?
(a) 293
(b) 345
(c) 414
(d) 690
(e) 828
Resolução
Inicialmente, é necessário calcular a massa de ácido acetilsalicílico (AAS) no lote de 900 mil comprimidos:
1 comprimido ——————– 500 mg
900000 comprimidos ————- X
X = 45 . 104 g de AAS
Em seguida, calcula-se a massa de ácido salicílico necessário considerando o rendimento final de 50%, sendo assim. 1 mol de ácido salicílico produz 0,5 mol de AAS:
138 g de ácido salicílico (1 mol) ————- 90 g de AAS (0,5 mol)
Y ————- 45 . 104 g
Y = 690 . 103 g = 690 kg
Resposta: D








