O que são íons?
Os íons são espécies químicas eletricamente carregadas por apresentarem número de elétrons diferente do número de prótons. Essa espécie química é resultante de uma perda ou de um ganho de elétrons durante algum processo.
O fato de uma espécie química se tornar um íon modifica as suas propriedades físicas e químicas. Um exemplo disso é o sódio. O sódio metálico (Na) é muito reativo e pode gerar explosões em contato com o meio aquoso. Por isso, o sódio presente nos alimentos como o NaCl está em forma de um íon positivo, Na+.
O que é a carga de um íon?
Os átomos em seu estado fundamental são eletricamente neutros, ou seja, o número de prótons que apresenta (carga relativa e positiva de +1) é igual ao número de elétrons com (carga negativa de -1) e assim, essas cargas se anulam. Diferentemente do que ocorre nos íons, já que não acontece esse anulamento.
Portanto, a carga de um íon está relacionada à diferença de prótons e elétrons existente na espécie química. Caso o íon apresente carga positiva, ele será um cátion, enquanto, a carga negativa, é característica de um ânion.
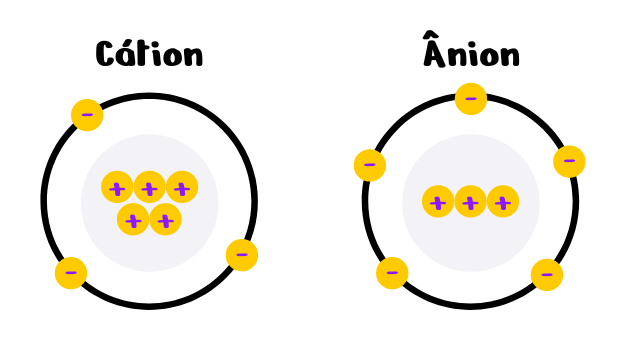
Cátion
Os cátions são átomos que perdem elétrons passam a ter um maior número de prótons em relação ao número de elétrons e por isso, o íon formado é um íon positivo uma vez que possui carga positiva.
Os cátions são formados, em geral, por átomos de metais alcalinos (IA) e alcalino terrosos (IIA).

Dependendo da carga positiva do íon, os cátions podem ser classificados em: monopositivos (+1), dipositivos (+2), tripositivos (+3) e tetrapositivos (+4).
Ânion
Os ânions são átomos que ganham elétrons, apresentam um número maior de partículas subatômicas negativas do que de prótons. Desse modo, o íon possui carga negativa.
Os ânions são classificados em: monovalente (-1), bivalente (-2), trivalente (-3) e tetravalente (-4).
O que é a ionização?
Ionização é o processo químico em que ocorre a formação de íons que não estavam anteriormente presentes no sistema.
A ionização pode ocorrer por meio de radiação ou em solução aquosa.
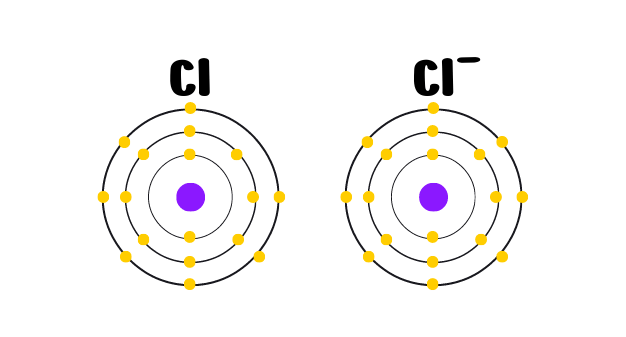
Em solução aquosa, ao adicionar uma molécula formada por ligação covalente em que há compartilhamento de elétrons, ocorre a formação de íons. Um exemplo é a adição de um ácido clorídrico à água.
Nesse caso, a água atua como reagente e retira o átomo de hidrogênio da molécula, como mostra a reação a seguir.
HCl + H2O → H3O+ + Cl–
Ligação iônica
A ligação iônica ocorre entre átomos que buscam a estabilidade para ficarem neutros. Segundo a Teoria do Octeto, isso ocorre quando os átomos atingem 8 elétrons na camada de valência.
Na ligação iônica, os elétrons são doados ou recebidos. Ou seja, um ânion se une a um cátion para que ocorra a formação do composto iônico. O que acontece nesse tipo de ligação é diferente do que ocorre na ligação covalente, onde há o compartilhamento de elétrons.
Porque alguns átomos tendem a perder elétrons enquanto outros tendem a ganhar elétrons?
De acordo com a Regra do Octeto, os átomos tendem a se combinar de forma que a sua camada de valência tenha 8 elétrons. Isso é devido à configuração dos gases nobres que são estáveis, em condições normais de temperatura e pressão, e apresentam configuração eletrônica com 8 elétrons na camada de valência.
Desse modo, elementos presentes na tabela periódica que possuam 5 ou mais elétrons na camada de valência tendem a ganhar elétrons, já que precisam de poucos elétrons para garantir a estabilidade. Esses elementos são encontrados nas famílias 5A, 6A e 7A.
Em contrapartida, átomos de elementos que tenham até 3 elétrons na sua camada de valência, possuem a tendência de perder esses elétrons. São os átomos encontrados nas famílias 1A, 2A e 3A.








